日本リウマチ財団ニュース
No.195号2026年3月号
国際学会報告書 アメリカリウマチ学会(ACR)2025
日本リウマチ財団ニュース195号に掲載しています「アメリカリウマチ学会(ACR)2025学会速報 」のロングバージョンです。
田巻 弘道 氏
聖路加国際病院 Immuno-Rheumatology Center 医長
責任編集:岡田 正人
財団ニュース編集部会部会員
聖路加国際病院 Immuno-Rheumatology Center
はじめに
ACR convergence 2025はシカゴで行われた。ACRの定番の場所のうちの一つであるMcCormick Placeである。アメリカらしい広いスペースの学会場での開催である。10月の終わりで、ハロウィーンを間近に控えカボチャの飾りを街で見かける雰囲気の中、木々も紅葉で色づき、日本であれば冬のような気温の中の開催であった。今回も非常に盛り上がった学会であったが、今回のACRの発表の中から、筆者が独断と偏見で興味深いと感じた内容を幾つか取り上げる。
1. ACRのSLEのガイドライン
米国リウマチ学会(ACR)は、全身性エリテマトーデス(SLE)に関する新たな診療ガイドラインを発表した。ループス腎炎を除く全身管理に関するガイドラインとしては1999年以来、実に26年ぶりの改訂となる。このセッションでは、まずは、Lisa Sammaritano医師による全般の説明から始まり、その後各臓器領域の実際への応用が話された。取り上げられた領域は、漿膜炎、皮膚、関節炎、小児であった。
ガイドラインの全般的な説明を行う。本ガイドラインはGRADEシステムを用いた厳格な手法、患者パネルからのインプット、および投票パネルによる合意形成を経て作成された。対象はループス腎炎を除くSLEの全般的管理および臓器別治療であり、人種や年齢に関わらず適用される。特筆すべき点は、全36のグレード付き推奨事項のうち「強い推奨(Strong Recommendation)」はわずか3つ(8%)にとどまり、残り33(92%)は「条件付き推奨(Conditional Recommendation)」であることだ。これは、ループス腎炎ガイドラインと比較してSLEの多くの領域で質の高いエビデンスが限定的であることを反映しており、実臨床における共同意志決定(SDM)の重要性が極めて高いことを示唆している。
治療の全体目標は、寛解または低疾患活動性の達成・維持による長期予後の改善と、治療関連毒性の最小化である。モニタリングについては、疾患活動性は定期的(臨床状態や薬剤変更時を含む)に、疾患損傷(ダメージ)については少なくとも年1回の評価を行うことが条件付きで推奨された。併存疾患の管理については、推奨事項の形式ではなくGood Practice Statement(GPS)として、スクリーニングと管理の重要性が強調されている。
薬物療法において「強い推奨」が含まれるのは、グルココルチコイド(GC)、ヒドロキシクロロキン(HCQ)、および難治例への対応である。GCに関しては、プレドニゾン換算で5mg/日を超える量で疾患が安定している場合、6ヶ月以内に5mg/日以下(理想的には中止)まで減量することが強く推奨された。これは低用量であっても長期投与による毒性リスクが蓄積するためである。また、持続的な寛解にある場合は、GCの中止に向けた緩徐な減量が条件付きで推奨されている。初期治療におけるGC毒性を最小限に抑えるため、早期から免疫抑制療法を導入・強化する戦略が支持されている。
HCQについては、禁忌がない限り全例でルーチンに使用することが強く推奨されている。また、持続的な寛解状態であっても治療を無期限に継続すること、および網膜毒性を最小限に抑えるために長期的な維持用量は5mg/kg/日以下を目指すことが条件付きで推奨された。免疫抑制療法に関しては、3~5年の持続的な寛解または低疾患活動性が維持された場合、中止を目標とした減量を考慮することが条件付きで推奨されている。
臓器特異的な治療推奨(皮膚、筋骨格、神経精神、血液、心血管など)については、エビデンスの不確実性や専門家間の診療パターンの多様性を背景に、すべてが「条件付き推奨」となっている。特定の薬剤の優劣をつけることが難しい領域も多いため、初期治療に抵抗性の場合は、漫然と継続するのではなく治療を強化するという原則が強く推奨されている。生命を脅かす臓器病変に対しては、パルス療法を含む強力な治療を緊急に行うべきとされる。
本ガイドラインは、多くの推奨が「条件付き」であることから、個々の患者の臨床的状況、価値観、選好を考慮した上で、医師と患者が協働して治療方針を決定するための指針として活用されるべきである。実際のガイドラインの全容に関しては表1を参照にしていただきたい。また。ガイドラインはすでにonline firstで発表されているので、そちらも確認いただけたらと思う。
表1)SLE ACRガイドライン2025


2. JIAのガイドライン
米国リウマチ学会(ACR)Convergenceにおいて発表された「2025年版 若年性特発性関節炎(JIA)治療ガイドライン(ドラフト版)」のセッションを解説する。本ガイドラインの改訂における特筆すべき点は、作成方法論が従来のRAND法からGRADEアプローチへと移行したことであり、これによりエビデンスの質のみならず、患者の価値観や選好、益と害のバランスがより色濃く反映された推奨が可能となった。また、薬剤の中止や離脱といった受動的な表現に代わり、医学的な管理下で計画的に薬剤を減量・中止するプロセスとして「Deprescribing(減薬)」という用語が採用された点も、長期管理を見据えた臨床的なパラダイムシフトを示唆している。
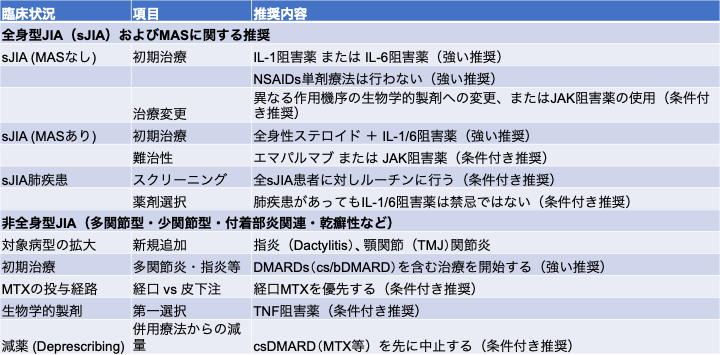
全身型JIA(sJIA)に関しては、2021年版と比較して推奨項目が大幅に拡充された。マクロファージ活性化症候群(MAS)を伴わない症例において、初期治療としてのIL-1阻害薬またはIL-6阻害薬の使用は、従来の「条件付き推奨」から「強く推奨」へと格上げされた。一方で、NSAIDs単剤による初期治療は「強く推奨しない」とされ、早期からの生物学的製剤導入による疾患制御の重要性が強調されている。MAS合併例においても、全身性グルココルチコイドに加えてIL-1/6阻害薬を併用することが「強く推奨」されており、難治性MASに対してはエマパルマブやJAK阻害薬の使用が新たな選択肢として明記された。さらに、近年注目されるsJIA肺疾患(sJIA-LD)については、既知のリスク因子の有無にかかわらず全例でルーチンのスクリーニングを行うことが条件付きで推奨されたほか、肺疾患の存在はIL-1/6阻害薬使用の絶対的禁忌とはみなされないとの見解が示されたことは、実臨床における治療選択に大きな影響を与えるものである。
非全身型JIA(多関節型、少関節型、付着部炎関連等)の領域では、対象疾患に指炎および顎関節(TMJ)関節炎が新たに追加された。治療戦略における最も大きな変更点の一つは、メトトレキサート(MTX)の投与経路に関する推奨の逆転である。従来はバイオアベイラビリティの観点から皮下注が推奨されていたが、今回はドイツのBIKERレジストリ等のデータに基づき、経口投与が皮下注よりも「条件付きで推奨」されるに至った。これは、皮下注における有害事象による中止率の高さや、経口投与でも同等の長期予後が得られる可能性、さらには患者負担の軽減を考慮した結果である。生物学的製剤については、多くの病型でTNF阻害薬が第一選択として推奨されている。また、Deprescribingの観点からは、生物学的製剤と従来型DMARD(csDMARD)の併用療法で寛解が維持されている場合、再燃リスクを考慮して、生物学的製剤よりも先にcsDMARDを減量・中止することが推奨された。生物学的製剤自体の中止に際しても、即座の中止ではなく漸減(tapering)を行うことが望ましいとされている。
JIAに伴うぶどう膜炎に関しては、視力予後の改善を最優先とするアグレッシブな介入方針が示された。高リスク患者に対する3ヶ月ごとの眼科スクリーニングが強く推奨されたことに加え、初期治療においては、慢性前部ぶどう膜炎と診断され局所ステロイドが必要となった時点で、待機期間を設けることなく直ちに全身的DMARD療法(MTX等)を開始することが条件付きで推奨された。これは2019年版で許容されていた3ヶ月の待機期間を撤廃するものであり、不可逆的な視機能障害を防ぐための早期介入の重要性を反映している。また、眼局所へのステロイド注射は初期治療として推奨されず、全身治療が優先される。生物学的製剤の選択に関しては、他の薬剤と比較してアダリムマブの使用が推奨されており、TNF阻害薬開始時には関節炎に対する標準用量よりも高用量での導入が考慮されるべきであるとされた。
最終的な承認を経た正式版の公開が待たれるところである。このセッションで触れられた推奨に関しては表2を参照にしていただければと思う。
表2)JIAのACRガイドライン

3. 自己免疫疾患治療の新たな地平:CAR-Tの限界を超え、精密T細胞エンゲージャー(TCE)の時代へ
自己免疫疾患治療は、CAR-T細胞療法が難治性SLEなどで劇的な有効性を示したことにより、大きな変革期を迎えている。しかし、ACR Convergenceにおけるジョンズ・ホプキンス大学のMaximilian F. Konig博士の講演は、我々の視線をCAR-Tの限界の先、すなわち「精密T細胞エンゲージャー(TCE)」という新たな地平へと向けさせるものであった。CAR-T療法は高い有効性を持つ一方で、B細胞の完全枯渇に伴う重篤な感染症リスク、IVIG補充を要する低ガンマグロブリン血症、そしてサイトカイン放出症候群(CRS)といった深刻な毒性を内包している。さらに、アフェレーシス、ブリッジング療法、高額なコストと製造の複雑性といった運用上の課題も依然として存在する。
これに対し、T細胞上のCD3とB細胞や形質細胞上の標的抗原(BCMA, CD19など)を橋渡しするバイスペシフィックTCEは、抗体ベースの「オフ・ザ・シェルフ(既製品)」製剤であり、細胞工学やリンパ球除去の前処置を必要としない点で、臨床応用における大きな利点を持つ。事実、BCMAを標的とするTCE(Teclistamabなど)は、すでにSLEや強皮症(SSc)患者において、皮膚硬化(mRSS)の改善や有望なバイオマーカーの変化を示し始めており、そのポテンシャルは明らかである。
しかし、Konig博士が指摘するように、これら既存のTCEの多くは腫瘍免疫領域からの「再利用(Repurpose)」であり、B細胞全体を枯渇させるという点において、CAR-Tと共通の課題、すなわち免疫不全と感染症リスクを依然として抱えている。博士は、自己免疫疾患治療として真に最適化するためには、薬剤を単に転用するのではなく、その病態に合わせて「リデザイン(Redesign)」する必要があると強く主張した。その戦略の核心は二つある。第一に、CD3への結合親和性(アフィニティ)を意図的に調整・低下させることでT細胞の過剰な活性化を抑え、CRSなどの毒性を低減すること。第二に、そして最も重要な点として、B細胞全体を無差別に攻撃するのではなく、病態を引き起こす「自己反応性細胞」のみを選択的に標的にし、正常なB細胞を温存することで、免疫不全と感染リスクを根本的に回避することを目指すものである。
この「精密免疫療法」を実現するための具体的なアプローチとして、いくつかの革新的な設計が提示された。例えば「BaiTE (Bispecific Autoantigen-T cell Engagers)」は、TCEの一方に自己抗原(例:APSにおけるB2GPI)を組み込むことで、その抗原に反応するB細胞受容体(BCR)を持つ細胞だけを選択的にT細胞に攻撃させる。また、SLE患者の自己反応性B細胞の多くが共通のIGHV4-34遺伝子セグメント(9G4イディオタイプ)を用いる知見に基づき、この9G4陽性B細胞集団のみを標的とするTCEも開発されている。さらに、強直性脊椎炎(AS)のようにT細胞が病態の主役となる疾患に対しても、HLA-B27陽性患者の病態駆動性CD8+ T細胞が共通して発現するTCR(TRBV9)を標的とするTCEが開発されており、病的なT細胞クローンのみを選択的に除去する試みが進んでいる。
結論として、TCEはCAR-T療法の運用上の課題を克服しうる強力な治療モダリティである。特に、自己免疫疾患の病態基盤に合わせて精密に「リデザイン」された次世代TCEは、病的な自己反応性細胞のみを選択的に除去することで、有効性を維持しつつ深刻な免疫不全を回避できる可能性がある。これは、寛解導入後の長期的な安全性確保や、より広範な患者層への適応拡大を可能にするかもしれない。リウマチ治療における次なるパラダイムシフトを牽引する技術として、その発展が大いに期待される。
4. Klemperer Lecture — RAの新しい病態理解と治療標的
ハーバード大学のMichael Brenner先生がACRのPaul Klemperer memorial lectureにおいて、「関節リウマチ(RA)およびその他の自己免疫疾患の免疫病態における新しいパラダイム」と題し、近年の高次元解析技術が明らかにしたRA病態の知見を発表した。
一つ目のパラダイムシフトとして、RAの病態の中心をなしているT細胞の理解が進んだことが述べられた。従来の考えではCD4陽性T細胞が病態形成の中心であり、その中でもTh1細胞(IFN-γ産生)やTh17細胞(IL-17産生)が主役と考えられてきた。Accelerating Medicines Partnership(AMP)コンソーシアムなどの大規模研究により、RA患者の滑膜組織で実際に拡大しているのは、これまで知られていなかった特殊なCD4 T細胞集団であることが判明した。この新しい細胞集団は「Tph細胞(T peripheral helper cells:末梢性ヘルパーT細胞)」と名付けられ、特に血清陽性RA患者の滑膜において、CD4 T細胞全体の約1/3という非常に高い割合を占めている。Tph細胞の際立った特徴は、PD-1を強く発現する一方で、従来のTfh(濾胞性ヘルパーT細胞)が持つCXCR5を発現していない点にある。彼らの主な役割は、リンパ節の胚中心ではなく、炎症が起きている末梢組織(すなわちRA滑膜)の「濾胞外」でB細胞と直接相互作用することである。Tph細胞はIL-21やCXCL13といったサイトカインを強力に産生し、B細胞を局所で強力に活性化させる。これにより、抗体産生細胞(形質芽球や形質細胞)への分化が促進され、ACPA(抗CCP抗体)に代表される自己抗体の産生が滑膜局所で駆動されていると考えられる。このTph細胞による局所的なB細胞活性化というメカニズムは、RAのみならずSLEやシェーグレン症候群など、他の多くの自己免疫疾患にも共通する病態基盤である可能性が示唆された。
CD4 T細胞と並び、これまでその役割が見過ごされがちであったCD8陽性 T細胞も、RA滑膜に豊富に浸潤していることが明らかとなった。驚くべきことに、従来Th1細胞の主な役割とされてきたIFN-γの産生は、RA滑膜においてはむしろCD8陽性 T細胞が主要な供給源であったことが示された。これらのCD8 T細胞の多くが、細胞傷害性に働くグランザイムBを産生するタイプではなく、「グランザイムK(GzmK)」という別のプロテアーゼを極めて高レベルで発現していたことである。GzmKのタンパク質構造は「補体因子D」と酷似しており、研究の結果、GzmKはC1sやMASP2(古典的経路やレクチン経路の開始酵素)と同様に、補体のC4とC2を直接切断し、C3転換酵素を形成できるという機能が判明した。GzmKは細胞表面のヘパラン硫酸に結合する性質を持つため、T細胞から放出されたGzmKは血中に拡散せず、細胞表面に留まり、組織局所で効率的に補体カスケードを駆動する。これにより、C3aやC5a(強力な炎症惹起・走化性因子)、C3b(オプソニン化)、さらには膜侵襲複合体(TCC)の形成まで、補体経路全体が活性化されることが示された。これは、抗体や免疫複合体を介さない「T細胞による直接的な補体活性化」という、全く新しい炎症メカニズムの発見である。GzmK欠損マウスが乾癬様皮膚炎モデルで症状と補体沈着の軽減を示したことから、GzmKはRAや乾癬など多くの炎症性疾患において、新たな治療標的となる可能性を強く示唆している。
次に示されたのが、線維芽細胞の理解の促進である。RAにおける組織破壊、すなわちパンヌス形成による軟骨破壊や骨びらんの実行犯は、滑膜線維芽細胞である。AMP研究により、RA滑膜では「CD90+の炎症性滑膜下線維芽細胞」が著しく拡大していることが確認された。この線維芽細胞の活性化・増殖のドライバーとして、血管内皮細胞から供給されるNotch3シグナルや、Wntシグナル(特にWnt5a)が重要な役割を果たしていることが突き止められた。研究はさらに、この線維芽細胞の複雑な振る舞いを統括する「マスター制御因子」の同定へと進んだ。その結果、2つの重要な転写因子が同定された。一つはRAのリスク遺伝子でもあるARID5Bである。ARID5Bは、線維芽細胞の炎症性サイトカイン産生を抑制する一方で、組織浸潤能を促進するという、二面性を持つ「スイッチ」として機能していることが示された。もう一つはETV7であり、こちらは線維芽細胞の活性化を「グローバルに(広範に)」抑制する強力なリプレッサー(抑制因子)として同定された。ETV7を過剰発現させると、IL-6、各種ケモカイン、MMPなど、炎症と破壊に関わる多くの遺伝子が一斉に抑制されたのである。
ブレナー博士の講演は、RAの病態が単一のサイトカインや細胞で説明できる単純なものではなく、Tph細胞による局所B細胞活性化、GzmK陽性CD8 T細胞による局所補体活性化、そしてNotch/Wntシグナルで活性化されARID5B/ETV7などで精密に制御される線維芽細胞が複雑に絡み合うネットワークであることを示した。これらの新しいパラダイムは、既存薬抵抗性の病態解明はもちろん、GzmK阻害剤、Notch/Wntシグナル阻害剤、あるいはETV7の誘導といった、全く新しい治療戦略の開発に道を開くものであり、今後のリウマチ診療に大きな影響を与える知見と言えるだろう。
5. Philip Hench Memorial Lecture
ジョン・ストーン教授によるフィリップ・ヘンチ記念講演は、「IgG4関連疾患(IgG4-RD):ベッドサイドからベンチ、そしてステロイドフリーの世界へ」と題し、本疾患の歴史的経緯から最新の病態解明、治療戦略までを網羅したものであった。
まず、IgG4-RDがステロイド治療に不向きな疾患である点を強調。ステロイドは寛解導入には有用だが、長期的な疾患制御には不十分(高率なフレア)であり、ステロイドフリー治療の確立が急務であるとした。
歴史的背景として、Mikulicz病や自己免疫性膵炎(硬化性膵炎)が独立した疾患として扱われていたが、濱野・河・神澤ら日本人研究者による血清IgG4高値の発見と全身性疾患概念の確立が決定的な転機となった経緯が概説された。
臨床的特徴として、多臓器にわたる線維化性病変、悪性腫瘍(癌)との鑑別の重要性に加え、「Indolent = DANGEROUS(緩徐進行=危険)」という臨床的概念を提示。無症候性に臓器障害が進行する点や、アトピー素因(喘息、アレルギー性鼻炎等)との強い関連性を指摘した。また、大動脈炎や冠動脈炎を含む「Variable vessel vasculitis」としての側面も強調された。
病態生理に関しては、B細胞とT細胞の異常な協調が核心にあるとした。IgG4産生は主に短寿命の形質芽細胞(Plasmablast)に由来し、リツキシマブ(抗CD20抗体)によるB細胞除去療法が有効な根拠となっている。さらに重要な知見として、TCR-Vβレパトア解析により、IgG4-RDの病巣にはクローナルに増殖した細胞傷害性T細胞(CTL)、特にCD4+GranK+およびCD8+GranK+ T細胞が浸潤していることが示された(Koga, JACI 2023)。これらのCTLsが線維化を誘導すると考えられている。加えて、Katz Gら(ACR 2025)やDoradoら(Nature 2025)の研究から、補体活性化(特に第四の経路)の関与も新たな病態として注目されている。
治療の展望として、B細胞除去療法の有効性を示したInebilizumab(抗CD19抗体)のNEJM掲載の臨床試験が紹介された。プラセボ群に対し有意にフレアを抑制し(ステロイド再開率 37% vs 10%)、ステロイドフリー維持の可能性を示した。今後は、B細胞抑制(inhibition)を目的とするObexelimab(CD19/FcγRIIb)やBTK阻害剤(Rilzabrutinib)など、詳細な病態に基づいた新規治療薬の開発が期待されると締め括った。
6. 個人的に興味を惹かれた発表や研究結果
【口演】
SELECT-GCAの2年目の結果(アブストラクト番号0766)
第3相前向き二重盲検ランダム化比較試験であるSELECT-GCA試験の最初の52週間(Period 1)において、ウパダシチニブ(UPA)15mgはプラセボ(PBO)と比較し、GCA患者の寛解率を有意に改善した。本研究は、52週の時点で24週間以上の連続寛解を達成した患者を対象とした試験である。Period 1でUPA 15mgを投与されていた患者は、UPA 15mgの継続、またはPBOへの切り替えに2:1で割り付けられ、52週から104週まで観察された。この解析は、UPA 15mgから継続投与された群(N=68)と、UPA 15mgからPBOに切り替えられた群(N=35)の比較に焦点を当てられている。52週から104週の主な有効性の結果としては、疾患増悪を1回以上経験した患者の割合は、UPA 15mg継続群(15.5%)の方が、PBO切替群(59.1%)よりも有意に(P<.001)少数であり、UPA 15mgを継続した患者は、PBOに切り替えた患者と比較して、疾患増悪のリスクが90%低減した(HR:0.10, P<.0001)。104週の時点で完全寛解(GCAの徴候・症状なし、GC不使用、ESRおよびhsCRP正常化)を達成した患者の割合は、UPA 15mg継続群(71.9%)の方が、PBO切替群(20.0%)よりも有意に(P<.001)高く、52週から104週までの累積GC(プレドニゾン換算)使用量の中央値は、UPA 15mg継続群(0 mg)が、PBO切替群(1048.0 mg)よりも有意に(P<.0001)少なかった。平均累積GC使用量も、UPA 15mg継続群(139.2 mg)がPBO切替群(1532.6 mg)より約1グラム少なく、GC減量効果を示した。2年間全体の安全性としては、本試験の患者集団(平均年齢約71歳)において、ウパダシチニブの長期使用による臨床的に重大な新たな安全性のシグナルは認められなかった。
抗MDA5抗体のエピトープによる予後予測(アブストラクト番号0773)
抗MDA5抗体陽性皮膚筋炎に伴う間質性肺疾患(ILD)は、既存の多剤併用療法に抵抗して急速に進行し、予後が極めて不良な例が多い。治療の個別化と早期の適切な介入を実現するためには、予後不良例を感度よく特定する指標が不可欠である。本研究では、MDA5分子上の特定のエピトープに対する抗体反応性が、ILDの臨床経過や重症度を予測する新たなバイオマーカーとなり得るかを検証した。まず、16名の発見コホートにおいてT7ファージディスプレイ解析を行い、MDA5分子のaa 201-300およびaa 601-700領域を主要なエピトープとして同定した。解析の結果、aa 201-300領域に対する高い反応性が、初期治療に対する抵抗性(死亡、あるいは血漿交換やJAK阻害薬等の強力な追加治療を要する状態)と統計学的に有意に関連していることが見出された。
この知見を84名の独立した検証コホートで評価したところ、aa 201-300陽性群の無増悪生存率は43%であり、陰性群の74%と比較して統計学的に有意に低かった(p = 0.001)。多変量Cox比例ハザードモデルによる解析では、年齢や血清フェリチン値などの既知の予後不良因子を調整した後も、aa 201-300反応性は独立した予後予測因子として残り、ハザード比(HR)は2.14(95%信頼区間[CI]: 1.15–3.98、p = 0.016)であった。
さらに、従来の抗MDA5抗体検査では陰性と判定される特発性間質性肺炎(IIP)患者288名においても、aa 201-300への反応性が生存予後を規定することが明らかになった。陽性例の5年生存率は32%であり、陰性例の66%と比較して有意に低かった(p < 0.0001)。これは、MDA5を介した免疫学的機序が皮膚筋炎の有無にかかわらず、広範なILDの予後に寄与していることを示唆している。病態機序としては、肺損傷により漏出したMDA5が自己抗原となり、特定のエピトープに対する抗体産生を介して炎症応答を増幅させ、肺の線維化を進行させている可能性がマウスモデル等の解析で示されている。aa 201-300に対するエピトープ特異的抗体の測定は、皮膚筋炎のみならず広範なILDの予後層別化において、治療戦略を最適化するための極めて有望なバイオマーカーである可能性がある。
細菌由来sRNAであるtDR-1増加によるハイリスク群での関節リウマチ進行低下(アブストラクト番号0775)
sRNAは、DNAから転写されたRNAがタンパク質に翻訳される過程において、Post-transcriptional regulationを行う分子であり、遺伝子発現の制御に重要な役割を担っている。RA患者において血中微生物由来sRNA プロファイルが変化していることが示されており、細菌由来sRNAが細胞外小胞を介して宿主細胞に作用しうるメカニズムや、生物間RNAコミュニケーションの可能性が知られている。
このグループの行った先行研究では、ヒト血漿中に存在するsRNAのうち約20%が微生物由来であることを明らかにした。その中で、細菌のアルギニンtRNAに由来する断片である tDR-1 を同定した。RA患者において、血漿中のtDR-1濃度が高いほど、圧痛関節数が少なく、DMARDに対する治療反応性が良好であることと関連していた。
今回の研究では、RA発症リスク研究のコホートから、ベースライン時点で抗CCP3抗体陽性でありRA未発症の被験者を追跡し、RAを発症した群 (n=25) と発症しなかった群 (n=35)、および健常対照群 (control, n=123) のベースライン血漿の微生物tDR-1濃度を測定した。
べースライン時点での血漿tDR-1濃度は、将来RAを発症した群において、発症しなかった群 および健常対照群 と比較して有意に低値であった。また、発症しなかった群は健常対照群よりも有意に高値を示した (p=0.004) RA発症予測能を評価するためROC解析では、既知のリスク因子(Shared epitope、喫煙歴、1種類以上のRF陽性)のみを用いたモデルのAUROCは0.74であった。一方、tDR-1濃度のみでもAUROC 0.86と高い予測能を示した。そして、既知のリスク因子にtDR-1濃度を加えたモデルではAUROCが0.91へとさらに有意に向上した。
さらに筆者らは、DR-1の生物学的機能を探るため、in vitro実験を行った。健常者の末梢血単核球 (PBMC) を単離し、合成したtDR-1 mimicまたは配列をランダム化したスクランブルコントロールRNA mimicで刺激した。刺激後の細胞からRNAを抽出し、免疫関連遺伝子579種類の発現量を網羅的に解析した。tDR-1刺激群では、コントロール群と比較して、多数の1型IFN応答関連遺伝子の発現が有意に低下していた。具体的には、STAT1、STAT2、IRF7、MX1、IFITM1、IFI16、IFI35、IFIH1、BST2 といったIFN誘導遺伝子やシグナル伝達因子、さらにB細胞の生存因子である TNFSF13B (BAFF) などの発現低下が認められた。
先行研究で、発症前段階の自己抗体陽性者において、末梢血中の1型IFNシグネチャースコアが高い群 (High IFN) は、低い群 (Low IFN) と比較して、有意にRA発症リスクが高いことが報告されている。今回のin vitro実験でtDR-1が1型IFN応答遺伝子を抑制したという結果は、tDR-1がRA発症前の病態において保護的に作用するメカニズムとして、この1型IFN経路の抑制が関与している可能性を示唆するものである。
プロテオミクスを用いた胎児房室ブロックの予測因子(アブストラクト番号0853)
Olinkプロテオミクス技術を用いた胎児房室ブロック(fAVB)の予測因子に関する研究成果である。新生児ループスの重篤な合併症であるfAVBは、母体の抗SSA/Ro抗体が胎盤を通過し、胎児心筋に不可逆的な炎症と線維化をもたらすことで生じる。しかし、抗体陽性妊婦のうち実際にfAVBを発症するのは2〜4%に過ぎず、従来の抗体価測定だけでは正確なリスク予測が困難であった。本研究は、母体血液中の微量タンパク質を網羅的に解析することで、この課題の克服を試みたものである。
研究チームは、PATCH試験およびSTOP BLOQ試験から得られたサンプルを用い、fAVB発症群13例と、背景をマッチングさせた非発症の抗体陽性群13例を比較した。約5,400種類のタンパク質を対象としたプロテオーム解析の結果、母体の臨床診断、すなわち全身性エリテマトーデスやシェーグレン症候群といった全身状態は、fAVBの発症リスクとは無関係であることが明らかとなった。これは、fAVBが母体の疾患活動性とは独立して進行する、胎児特有のプロセスであることを強く示唆している。解析における最大の発見は、fAVB発症群の母体において、炎症性サイトカインであるIL-6が16倍以上、CCL3が8倍以上も有意に上昇していた点である。
これらのタンパク質の上昇は、fAVBが臨床的に診断される約1ヶ月前から確認されており、発症を事前に予知するバイオマーカーとして極めて有望である。さらに、死亡胎児の体液解析からも同様のサイトカインが検出されたことは、これらが胎児由来の炎症反応を反映し、胎盤を介して母体循環へ漏出していることを裏付けている。臨床的な展望として、抗体の胎盤通過を阻害するFcRn阻害薬ロザノリキシズマブを用いた治療例が提示され、高リスク妊婦におけるサイトカインの抑制と、健康な児の出産という成功例が示された。本研究は、IL-6とCCL3がfAVBの強力な予測因子であることを実証し、これに基づいた早期介入やFcRn阻害という新たな治療戦略に光を当てた。今後は大規模な多施設共同試験を通じて、これらの知見の臨床実装に向けた検証が進むことが期待される。
ASAS-SPARTAN改訂体軸性脊椎関節炎の分類基準(アブストラクト番号0854)
ASAS(Assessment of SpondyloArthritis international Society)およびSPARTAN(Spondyloarthritis Research and Treatment Network)による、体軸性脊椎関節炎(axSpA)の新たな分類基準「2025 ASAS-SPARTAN改訂分類基準」の開発とその検証結果についての発表である。
本改訂の背景には、既存の2009年ASAS分類基準における特異度の低さと、それに起因する偽陽性や過剰診断への懸念があった。特にX線学的変化を伴わないaxSpA(nr-axSpA)において、診断の不確実性が生物学的製剤の不適切な使用につながる可能性がFDA等から指摘されていた。これを受け、新たな基準の策定と検証を目的とした国際的な前向きコホート研究「CLASSIC試験」が実施された。本試験は世界27カ国から、45歳未満で発症し3ヶ月以上続く未診断の腰痛患者1,015名を登録し、画像の中央判定を含む全情報を参照したリウマチ専門医による診断をゴールドスタンダードとして解析が行われた。
検証の結果、2009年基準の感度は良好であったものの、特異度は施設内画像判定を用いた場合で約77%、中央判定を用いても約84%にとどまり、事前に設定された目標値(特異度90%以上)を達成できなかった。特に、機械的腰痛の有病率が高いプライマリケア設定等を考慮すると、特異度の向上は必須課題であった。そこで、LASSO回帰分析等のデータ駆動型アプローチを用いて、診断に独立して寄与する変数の抽出と重み付けが行われた。
新たに策定された2025年改訂基準は、画像・遺伝子領域と臨床症状領域の変数を組み合わせたスコアリングシステムを採用しており、合計11点以上を「axSpAとして分類」のカットオフ値としている。本基準の最大の特徴は、MRIによるaxSpA示唆所見(仙腸関節の骨髄浮腫等)に対して「7点」という極めて高い重み付けがなされた点である。これに対し、X線学的仙腸関節炎およびHLA-B27陽性はそれぞれ4点、炎症性腰痛は3点、その他の脊椎関節炎徴候(末梢関節炎、ぶどう膜炎、IBD等)は各1点と配点された。
この配点システムにより、MRI所見が陽性であれば、HLA-B27陽性(4点)のみの追加で合計11点となり基準を満たすことが可能である。一方で、画像所見(MRIおよびX線)が陰性の場合、HLA-B27が陽性(4点)であっても、炎症性腰痛(3点)に加え、さらに4つ以上の臨床徴候(各1点)がなければ11点に到達しない。これは、画像所見陰性かつHLA-B27陰性の症例は実質的にaxSpAとして分類されないことを意味し、特異度を優先した設計思想が反映されている。
最終的にこの新基準は、検証コホートにおいて感度75%以上かつ特異度90%以上という目標を達成した。質疑応答において、アフリカ系などHLA-B27陽性率が低い集団における適用性が懸念されたが、演者はMRI所見への高い配点がそのギャップを補完し、人種差によらず適切な分類が可能であるとの見解を示していた。本改訂基準は、臨床試験への適切な患者組入れを担保することが期待される。実際の分類基準は表3を参照にしていただきたい。
表3)2025 ASAS-SPArtan Revised Classification Criteria for AxSpA

GCAにおけるメトトレキサートとトシリズマブの比較試験(アブストラクト番号0891)
METOGIA試験はFrench Vasculitis Study Groupが行った前向き非盲検ランダム化比較非劣性試験であり、巨細胞性動脈炎(GCA)治療におけるメトトレキサート(MTX)をトシリズマブ(TCZ)と比較した試験である。MTXのTCZに対する非劣性マージンは20%に設定された。活動性GCAの患者(診断後6週以内)が対象で、無作為にTCZ 162 mg/週を52週間皮下投与 + プレドニゾン漸減かMTX 0.3 mg/kg/週(最大20 mg)を52週間皮下投与 + プレドニゾン漸減に振り分けられ、グルココルチコイドは##の段階で中止、 TCZおよびMTXは52週で中止されている。主要評価項目は 78週の時点で、再発またはプレドニゾンの規定漸減スケジュールからの逸脱がなく生存している患者の割合である。230名の患者が登録され(TCZ群 116名、MTX群 114名、主要評価項目の解析(PP解析)は196名(TCZ群 103名、MTX群 93名)で行われた。主要評価項目(78週時点)を達成した患者の割合は、TCZ群 51% 、MTX群 39%であり、両群の差は 12% (95%信頼区間: -2%~26%)であった。信頼区間の上限(26%)が事前に設定した非劣性マージン(20%)を超えたため、MTXのTCZに対する非劣性は示されなかった。また、信頼区間の加減はゼロをまたいでいる。副次評価項目(52週時点 – 薬剤投与中)としては、プレドニゾンなしでの寛解達成率がTCZ群 85%であるのに対しMTX群は62% (P=0.0002)、また、再発なくGC漸減スケジュールを逸脱しなかった割合はTCZ群で79%出会ったのに対しMTX群56%(P=0.0007)であった。この試験では78週時点での死亡例は、TCZ群で1名(1%)であったのに対し、MTX群では6名(6%)であり、特にMTX群では5例のニューモシスチス肺炎が報告され(うち1例は致死的、MTX使用によるPCPのリスク増加が示唆された。
早期関節リウマチ治療におけるTNF阻害薬を初期導入はD2TRAを減らせるのか(アブストラクト番号1677)
関節リウマチ(RA)診療において、既存の治療戦略で十分な改善が得られない難治性(Difficult-to-treat: D2T)RAへの移行をいかに防ぐかは、長期予後を左右する重要な課題である。本研究は、未治療の早期RA患者342名(平均年齢約50歳、罹病期間約6ヶ月)を対象に、初回治療としてTNF阻害薬(TNFi)を導入するステップダウン戦略が、長期的なD2T RAの発症率や臨床的寛解、および医療資源の利用状況に及ぼす影響を最長15年にわたり追跡調査したものである。解析対象は、初回12ヶ月間にTNFi(インフリキシマブまたはエタネルセプト)とメトトレキサート(MTX)を併用した導入群114名と、従来型DMARD(csDMARD)による標準的なTreat-to-target(T2T)を行った群228名である。
統計的解析の結果、主要評価項目である5年時点のD2T RA有病率は、TNFi導入群で1%未満(0%)であったのに対し、csDMARD群では7%であり、TNFi導入による有意なリスク低減が認められた(オッズ比 0.11、95%信頼区間[CI]: 0.01-0.88、p=0.037)。10年時点および最終フォローアップ時点(TNFi導入群:中央値167ヶ月、csDMARD群:中央値143ヶ月)においても、D2T RAの割合はTNFi導入群でそれぞれ6%、8%と、csDMARD群の11%、13%に比して数値的に低い傾向を維持したが、この時点での有意差は消失していた。しかし、持続的寛解率においては長期にわたる顕著な優位性が確認された。10年時点での寛解率はTNFi導入群が62%に対しcsDMARD群は45%(オッズ比 1.91、95%CI: 1.13-3.22、p=0.016)、最終フォローアップ時点では68%対48%(オッズ比 2.64、95%CI: 1.59-4.47、p=0.0002)となり、初期介入の効果が超長期にわたって持続することが示された。
医療経済面および治療強化の推移についても、TNFi導入群の優位性が統計的に裏付けられている。年間外来受診回数はTNFi導入群で2.5回、csDMARD群で3.3回であり、調整後の年間受診回数および関連コストの削減率は20%に達した(95%CI: -28.4%~-9.6%、p<0.001)。特筆すべきは、D2T RAに移行した症例の年間受診回数が6.2回と著しく高く、コストも増大していた点である。また、治療開始12ヶ月以降にbDMARDへの追加・強化が必要となるまでの期間をハザード比(HR)で評価すると、TNFi導入群は0.66(95%CI: 0.47-0.92、p=0.02)であり、csDMARD群と比較してbDMARDの再導入を平均11ヶ月遅延させることが可能であった。
以上のデータは、RA発症早期の「Window of Opportunity」においてTNFiによる強力な介入を行うことが、単なる症状緩和にとどまらず、D2T RAへの移行阻止をもたらす可能性を示唆している。バイオシミラーの台頭により経済的障壁が低下している現状において、初手から生物学的製剤を投入する戦略は、D2T RAに伴う患者の身体的苦痛と社会的・経済的損失を回避するための極めて合理的な選択肢となり得るかもしれない。さらなる追試が待たれるところであろう。
ヒドロキシクロロキンの血中濃度(アブストラクト番号1722)
全身性エリテマトーデス(SLE)治療においてヒドロキシクロロキン(HCQ)は、疾患活動性の抑制および臓器障害の蓄積予防に寄与する極めて重要な薬剤である。しかしながら、その至適投与量に関しては長年の議論が存在する。現行のガイドライン等では、網膜症リスクを回避するために体重あたり5mg/kg以下の投与が推奨されているが、最近の知見では、この用量制限がSLEのフレアリスクを2〜6倍に増加させ、入院率の上昇につながる可能性が示唆されている。一方で、5mg/kgを超える用量は確実に網膜毒性のリスクを高めるため、臨床医は有効性と安全性の狭間でジレンマを抱えているのが現状である。
HCQの薬物動態は、腎機能、薬物相互作用、細胞内代謝など多岐にわたる因子に影響を受けるため、従来の体重に基づく投与設定では大きな制限があり、血中濃度の個体差を制御できず、治療反応性の不均一性を招く。そこで本演題では、血中濃度モニタリングを用いた精密医療(Precision Monitoring)への転換が提唱された。具体的には、SLICCコホート、ウィスコンシンコホート、およびフランスの3つのコホートから得られた計1842例のデータを統合し、HCQ血中濃度の上限閾値の検証および高リスクサブグループの特定が行われた。
解析の結果、HCQ血中濃度の安全性と有効性を両立する治療域として、750〜1150 ng/mLという範囲が提示された。従来より750 ng/mL以上が治療効果発現に必要であることは知られていたが、本研究では特に上限値(1150 ng/mL)の臨床的意義が明確化された。血中濃度が1150 ng/mLを超える群では、それ以下の群と比較して網膜症のリスクが約2倍(オッズ比2.09)に上昇することが示された一方で、SLE疾患活動性(SLEDAI-2K 6以上と定義)の抑制効果に関しては、1150 ng/mLを超えてもさらなる上乗せ効果は認められず、治療効果が頭打ちになる(Ceiling effect)ことが確認された。すなわち、1150 ng/mLを超える血中濃度は「過量(Supratherapeutic)」であり、臨床的ベネフィットを伴わずに毒性リスクのみを増大させる領域であると結論付けられた。
さらに、HCQクリアランスの65%を腎臓が担っていることから、腎機能障害(CKD)の影響についても詳細な検討がなされた。解析の結果、CKDステージ3以上(eGFR 60未満)の患者では、腎機能が正常な患者と比較して、過量かつ毒性域の血中濃度となるオッズが2〜3倍に上昇することが判明した。特筆すべきは、体重あたり5mg/kg以下という推奨用量を遵守している場合であっても、CKDステージ3以上の患者においては、依然として血中濃度が過量域に達するリスクが有意に高いという点である。これは、腎機能低下例においては、現行の体重換算のみによる用量調節では不十分であり、過剰投与による毒性リスクに晒されている可能性を強く示唆している。
結論として、SLE診療におけるHCQの使用法について、従来の体重に基づく「一律的な」投与戦略から脱却し、血中濃度測定に基づく「個別化された」投与設計へ移行すべき時期に来ていると強調していた。特に、至適濃度域である750〜1150 ng/mLをターゲットとし、CKDステージ3以上の患者においては体重換算量に関わらず血中濃度モニタリングを積極的に行うことが、網膜症リスクを最小限に抑えつつ疾患活動性を制御するために推奨される。本研究は、長期間の追跡データと多施設共同研究に基づいており、実臨床におけるHCQの適正使用の重要性を再認識させる重要な報告である。残念ながら、現在の日本ではヒドロキシクロロキンの血中濃度測定は保険診療では行えない。
関節リウマチと大気汚染(アブストラクト番号1748)
関節リウマチ(RA)の免疫病態において、遺伝的素因に加えて大気汚染などの環境要因が重要視されている。本研究は、大気汚染物質がRAの疾患活動性およびフレア発生に及ぼす影響を評価することを目的として、ソウル大学病院において2021年1月から2024年12月までの期間に前向きコホート研究を実施した。解析対象は、2010年ACR/EULAR分類基準を満たし、6ヶ月以上の追跡および2回以上の外来受診歴を有する1070名の患者である。臨床データとして、DAS28-CRPやCDAI、ステロイドやDMARDsの使用状況が収集された。一方、大気汚染データについては、韓国国立環境研究院から提供された二酸化硫黄、二酸化窒素、オゾン、一酸化炭素、PM10、PM2.5の月間平均濃度を、各患者の居住地および受診時期に基づいてマッチングした。
統計解析には、患者内での繰り返し測定を考慮した一般化推定方程式(GEE)を用い、年齢、性別、喫煙歴、血清学的状態、薬物療法、ならびに気温や湿度といった気象因子を調整変数として含めた。さらに、感度分析として症例クロスオーバー(Case-Crossover)デザインを用い、同一患者内での高疾患活動性時期(ハザード期間)と低疾患活動性時期(コントロール期間)における曝露レベルの比較を行った。
結果として、対象となった1070名の平均年齢は61.3歳、女性が86.2%であり、4年間の追跡期間中に合計12,583回の受診、1,278件のフレアが記録された。多変量GEE解析の結果、特にPM2.5の濃度上昇がRAフレアの発生リスクと有意に関連していることが示された。また、PM10およびPM2.5の高濃度曝露はDAS28-CRPの上昇と有意に相関し、PM2.5についてはCDAIの上昇とも有意な関連を認めた。症例クロスオーバー分析では、関節炎フレア発生前の3週間以上にわたる期間において、PM2.5濃度がコントロール期間と比較して有意に高いことが明らかになった(p < 0.05)。
PM2.5は微細な粒子であるため肺胞深部まで到達して全身循環に入り、炎症や酸化ストレスを誘発することでRAの病勢増悪に関与している可能性が高い。本研究は、高レベルの大気汚染、とりわけPM2.5への曝露がRA患者の疾患活動性の悪化およびフレアの主要なリスク因子であることを裏付けている。特に3週間以上の累積的な曝露が臨床的な病勢変化に重要であることが示されており、RA診療において患者の居住環境や大気質に対する注意喚起が重要となることを示唆している。
EGPA維持療法におけるリツキシマブとアザチオプリンの比較(アブストラクト番号1765)
好酸球性多発血管炎性肉芽腫症(EGPA)における寛解維持療法の最適化を目的としたMAINRITSEG試験は、リツキシマブ(RTX)とアザチオプリン(AZA)を直接比較した初の第3相ランダム化二重盲検試験である。本試験では、新規診断または1年以内に再燃を認めたEGPA患者計98名が登録され、RTX群(49名)とAZA群(49名)に1対1で割り付けられた。RTX群には500mgを計5回(Day 1, 15, 6ヶ月後, 12ヶ月後, 18ヶ月後)投与し、AZA群には2mg/kg/日を24ヶ月間継続投与するプロトコルが用いられた。
主要評価項目である28ヶ月間のフォローアップ期間中における寛解(BVAS 0かつプレドニゾロン 7.5mg/日以下)の平均維持期間は、RTX群で98.4週(95%CI: 91.9-104.8)、AZA群で100.2週(95%CI: 94.6-105.8)であり、両群間に統計学的な有意差は認められなかった(p=0.82)。また、血管炎の再燃率についても、RTX群で14.3%(7/49名)、AZA群で18.4%(9/49名)とほぼ同等であった。EGPA特有の臨床像である喘息や鼻副鼻腔症状の再燃率に関しても、RTX群で44.9%(22/49名)、AZA群で42.9%(21/49名)と依然として高頻度であり、B細胞枯渇療法が好酸球性炎症の抑制においてAZAを凌駕する結果は得られなかった。
さらに、ステロイド節約効果を評価する指標である累積グルココルチコイド投与量の中央値は、RTX群で4,598mg、AZA群で4,591mgとほぼ同一であり、RTXによる追加の節約効果は証明されなかった。安全性については、重篤な有害事象(SAE)の発現率はRTX群で49.0%、AZA群で40.8%であった。特に注目すべきは重症感染症(Grade 3以上)の発生数であり、RTX群で23件と、AZA群の12件と比較して約2倍の件数が報告された。以上の結果から、EGPAの寛解維持においてRTXはAZAに対して優越性を示すには至っておらず、特にANCA陰性例や好酸球性炎症が主体となる病態に対しては、B細胞標的療法のみでは不十分である可能性が示唆される。本試験の結果は、GPA等で確立されたRTXの標準的地位をそのままEGPAに適用することの難しさを示しており、今後はIL-5阻害薬等との併用療法を含めた、病態に応じた個別化治療戦略の確立が不可欠である。
乾癬性関節炎に対する食事介入のランダム化比較試験(アブストラクト番号2690)
乾癬性関節炎(PsA)患者における食事介入の有効性を検証したランダム化比較試験DIPSAの結果が報告された。
本研究は、肥満を合併することが多いPsA患者に対して、特定の食事療法が疾患活動性の改善に寄与するかを明らかにすることを目的として実施された。背景には、肥満が治療抵抗性や症状の悪化と密接に関連している一方で、PsAに特化した食事介入のエビデンスが乏しいという現状がある。研究チームは、地中海食(MED)が持つ抗炎症作用に着目し、体重減少効果を超えた疾患活動性の改善が期待できるとの仮説を立てた。
試験デザインは多施設共同ランダム化比較試験であり、カナダと米国の計3施設において、中等度の疾患活動性を有するPsA患者を対象とした。介入群は、管理栄養士による個別指導を受ける地中海食群(MED群)と低カロリーのDASH食群(LC-DASH群)、および標準的な健康指導のみを行う対照群の3群に割り付けられた。主要評価項目は、開始12週目におけるDAPSA(Disease Activity Index for PsA)スコアの変化量とした。
試験の結果、開始24週目までに全群においてDAPSAスコア、圧痛関節数、および患者報告アウトカム(痛み、QOL、疲労感)の有意な改善が認められた。しかしながら、特定の食事介入による有意差は確認されず、地中海食群が他の群を上回るベネフィットを示すことはなかった。また、高感度CRP値については全群で有意な変化は見られなかった。
本研究の特筆すべき知見は、アウトカムの改善が特定の食事内容よりも、むしろ体重減少の程度と強く相関していた点である。DAPSAスコアや圧痛関節数、痛みの改善量は、減少した体重の割合に比例しており、臨床的に有意とされる5%以上の体重減少を達成した患者において、より顕著な症状改善が観察された。このことは、PsAの管理において、食事の組成そのものよりも、適切なエネルギー管理による減量維持が優先されるべきであることを示唆している。
一方で、標準的な指導のみを受けた対照群においても予想外の改善が見られた点は興味深い。これは、治験に参加し管理栄養士と面談すること自体が、患者の健康行動に変容を促し、食事習慣の適正化につながった可能性を反映している。本研究にはサンプルサイズの制約や、食事へのアドヒアランスのばらつきといった限界も存在するが、PsA診療における減量の重要性を再確認する重要なデータを提供したと言える。今後は、腸内細菌叢の変化や代謝プロファイルが疾患活動性に与える機序について、さらなるバイオマーカー解析による詳細な検討が期待される。
以上のように、PsA患者に対する食事介入においては、特定の食事療法に固執するよりも、まず持続可能な減量を主眼に置いた指導を行うことが肝要である。
個別化された体軸性脊椎関節炎に対する運動療法(アブストラクト番号2692)
体軸性脊椎関節炎(axSpA)は、仙腸関節や脊椎を中心に慢性炎症を起こす疾患であり、体幹の可動域制限や筋力低下、さらには心肺機能の低下を引き起こす。運動療法は非薬物療法の柱としてガイドラインで強く推奨されているが、その多くは一般人口向けのWHO基準に準拠した抽象的な指示に留まっており、個々の患者の身体能力や障害の程度に最適化された具体的なトレーニング指標は確立されていない。本研究「iSMART」は、客観的なベースライン評価に基づき、個別化した体幹機能訓練および有酸素運動を組み合わせた介入プログラムの効果を検証することを目的とした。
研究手法として、30名のaxSpA患者を対象に、週2回、計8週間の監視下トレーニングを実施した。介入前後の評価には、最大心肺運動負荷試験(CPET)と、代償動作を最小限に抑えるよう設計されたDavid Back Conceptデバイスによる体幹機能測定を用いた。プログラムの構成はデータ駆動型であり、有酸素運動はCPETで算出された第1換気閾値(VT1)時の心拍数を基準に強度を設定し、体幹トレーニングは1レップ最大重量(1RM)の30〜55%の負荷で、屈曲、伸展、側屈、回旋の4方向について個別に最適化された。
介入の結果、体幹筋力は測定した全4方向において有意な改善が認められた。可動域についても、伸展を除く3方向で有意な向上が確認され、特に屈曲や回旋での改善が顕著であった。心肺機能パラメータにおいても、酸素脈や換気効率、無酸素性作業閾値などの多くの指標が8週間という比較的短期間の介入で有意に向上した。臨床指標においては、患者報告アウトカムであるBASDAIに有意な改善が見られたが、BASFIやBASMI、胸郭拡張差については統計学的な有意差には至らなかった。
本研究の新規性は、CPETによる最大負荷試験と精密な体幹筋力測定を組み合わせ、客観的データに基づいて「テーラーメイド」の運動処方を行った点にある。これにより、患者個々の初期体力レベルに応じた段階的な負荷調整が可能となり、効率的かつ安全なリハビリテーションが実現された。課題として、小規模な単群研究であることや、運動介入を好む患者に偏る選択バイアスの可能性が挙げられるが、個別化された集中訓練がaxSpA患者の身体機能を底上げする有効な手段であることが示された。今後は、これらの改善効果を長期的に維持するための行動変容のアプローチや、臨床現場で実装可能な個別化ガイドラインの策定が期待される。
難治性関節リウマチに対する第1相CAR-Treg細胞療法(アブストラクト番号LB23)
難治性関節リウマチ(RA)を対象とした自己CAR-Treg細胞療法(SBT-77-7101)の第1相臨床試験「Regulate-RA」の中間報告である。SBT-77-7101は、シトルリン化ペプチド(CitP)を標的とするキメラ抗原受容体(CAR)を導入した制御性T細胞(Treg)であり、炎症部位における特異的な免疫抑制と組織修復の促進を目的としている。RA病態に特徴的なCitPを標的とすることで、治療細胞を炎症局所へ集積させる点が最大の特徴である。
製造工程では、患者自身の末梢血からアフェレーシスによりTregを分離し、レンチウイルスベクターを用いてCARを発現させた後、体外増殖を経て再投与する。特筆すべきは、従来のCAR-T細胞療法で一般的である投与前のリンパ球枯渇療法を必要としない点である。試験は3+3の用量漸増デザインで実施され、対象は3種類以上の作用機序が異なる生物学的製剤や標的型合成DMARDSに抵抗性を示す、難治性の症例に限定されている。
安全性に関しては、コホート2までの段階で用量制限毒性(DLT)は認められず、サイトカイン放出症候群(CRS)や免疫細胞関連神経毒性症候群(ICANS)の報告もない。有害事象の多くは軽度から中等度の一過性のものであり、主な症状は悪心、嘔吐、頭痛であった。1例で投与直後の関節痛および筋肉痛の増悪が認められたものの、全体として忍容性は極めて良好と判断されている。
有効性の探索的評価において、投与4週時点で6名中4名に腫脹・圧痛関節数の50%以上の減少が確認された。疾患活動性指標であるDAS28-CRPやCDAIにおいても、低用量群と比較して高用量群でより深く持続的な改善が認められ、機能障害を評価するHAQ-DIスコアも有意な改善を示した。これは、既存治療でコントロール困難であった患者群におけるADLの劇的な回復を示唆している。
薬理学的解析では、末梢血中のCAR-Treg細胞が最長18週間にわたって検出され、そのTregとしての表現型が維持されていることが示された。また、投与4週後の滑膜組織生検により、炎症性細胞浸潤の減少とともに、CAR陽性かつFoxP3陽性の細胞が患部に集積(ホーミング)していることが組織学的に証明された。これらの知見は、SBT-77-7101が炎症局所で標的特異的に作用し、免疫学的寛容を再構築している可能性を裏付けるものである。現在、さらに高用量での評価を行うコホート3が進行中であり、本療法の最適化と実用化に向けた進展が期待される。
イアナルマブのシェーグレン病に対する効果(アブストラクト番号LB24)
シェーグレン症候群(SjD)は、B細胞の過剰活性化とBAFF/BAFF受容体経路の異常を病態の核とする全身性自己免疫疾患であるが、未だ承認された標準的な全身療法は確立されていない。イアナルマブ(Ianalumab)は、糖鎖改変(Afucosylated)を施した完全ヒト型IgG1モノクローナル抗体であり、ADCCによる迅速なB細胞除去と、BAFF受容体遮断によるB細胞の活性化・生存抑制という独自の二重機序を有する。本報では、中等度から高度の活動性を有するSjD患者を対象とした2つの第3相国際共同試験(NEPTUNUS-1およびNEPTUNUS-2)の統合的解析結果を概説する。
両試験は、ACR/EULAR 2016分類基準を満たし、ESSDAIスコアが5以上の活動性を有する成人患者を対象とした。NEPTUNUS-1ではイアナルマブ300mg毎月(QM)皮下投与群とプラセボ群を1:1で、NEPTUNUS-2では300mg QM群、300mg 3ヶ月毎(Q3M)群、プラセボ群を1:1:1で割り付けた。主要評価項目は、投与48週時におけるESSDAIのベースラインからの変化量である。解析の結果、主要評価項目は両試験ともに達成された。48週時におけるESSDAI変化量の最小二乗平均値は、NEPTUNUS-1のQM群で-6.4(対プラセボ差 -3.8、p<0.0001)、NEPTUNUS-2のQM群で-6.5(対プラセボ差 -3.5、p<0.0001)と、いずれもプラセボ群(それぞれ-2.5、-3.0)に比して統計学的に有意な改善を示した。統合解析においてもQM群の改善は-6.5(対プラセボ差 -3.8、p<0.0001)であり、極めて強固なエビデンスが示された。また、NEPTUNUS-2におけるQ3M群の変化量は-5.0とプラセボとQM群の中間であり、明らかな用量依存性が確認されている。
副次評価項目においても臨床的に有意義な改善が認められた。48週時の低疾患活動性(ESSDAI < 5)達成率は、統合解析でQM群45.4%、プラセボ群24.4%であった。PhGA、PtGA、ESSPRIといった患者報告アウトカム(PRO)についても、QM群では投与4週から早期かつ持続的な改善傾向が確認された。特に注目すべきは、ベースラインで刺激時唾液流量(sSF)が0.4 mL/min以上維持されていたサブグループにおいて、QM群でsSFの有意な増加と口腔乾燥ドメイン(ESSD)の改善が認められた点であり、早期介入による外分泌機能の保持効果が示唆された。
安全性に関しては、イアナルマブの忍容性は良好であり、有害事象(AE)および重篤な有害事象(SAE)の発現率はプラセボ群と同等であった。統合解析における重篤な感染症の頻度はQM群1.3%、プラセボ群0.9%であり、悪性腫瘍等の重大な懸念も認められなかった。以上の知見から、イアナルマブは活動性シェーグレン症候群において、客観的疾患活動性と主観的症状の双方を有意に改善し、安全性プロファイルを有する画期的な治療薬になり得ると結論付けられる。
【ポスター】
関節リウマチにおけるクローン性造血(CHIP)の関係(ポスター番号0091)
関節リウマチ(RA)患者におけるクローン性造血(CHIP)は、一般人口と比較して高頻度に認められ、治療反応性や予後に深く関与している。本研究では、未治療のRA患者112名を対象に解析を行った結果、28%にクローン性造血(CH、VAF > 0.5 %)、10%にCHIP(VAF≧2%)が確認された。RAの慢性炎症環境がDNMT3A、TET2、ASXL1等の体細胞変異を持つクローンの増殖を促し、それが更なる炎症を惹起する自己増殖的なループを形成すると推察される。
臨床的な影響として、高疾患活動性(DAS28-ESR ≧5.2)を呈する患者において、CHIPの存在は治療反応性の低下と相関し、6ヶ月時点での無反応率はCH保有群で50%に達した(非保有群は22%)。また、CHはRA診断後の心血管イベント(OR 6.1)や悪性腫瘍(OR 6.9)の発生リスクを有意に高める要因であった。特に複数の変異を持つ症例では心血管疾患や癌の合併が多く、一部で骨髄単球性白血病(CMML)への進展も認められた。以上の結果から、RA診療においてCHIPは難治性や心血管・悪性腫瘍リスクを予測する重要なバイオマーカーとなり得る可能性がある。
グルココルチコイドの投与経路によるステロイド離脱率(ポスター番号1355)
本研究は、カナダの早期関節リウマチ(ERA)コホートであるCATCHを用い、発症初期3ヶ月間における副腎皮質ステロイド(GC)の投与経路が、12ヶ月後のGC離脱および高度標的治療(生物学的製剤やJAK阻害薬)導入に及ぼす影響を検討したものである。2023年のEULAR勧告ではGCの用量と期間を最小限に留める重要性が強調されているが、投与経路が総曝露量や離脱率に与える影響は十分に解明されていなかった。対象患者2,222名における多変量解析の結果、12ヶ月時点でのGC継続率は初期経口群で47%であったのに対し、非経口群(筋注または関節内注射)では26%と有意に低かった。ベースラインの疾患活動性(CDAI)や背景因子を調整した12ヶ月時点のGC継続オッズ比は、GC未使用群を基準として経口群で9.8、非経口群で4.1であり、初期に非経口投与を選択することは経口投与と比較してステロイド離脱の可能性を約2倍高めることが示された。一方で、12ヶ月時点での高度標的治療への移行率は両群間で同等(約14%)であった。以上より、ERAの初期治療において非経口GCを使用することは、治療強化のリスクを増大させることなく、円滑なステロイド離脱を促進する有効な戦略となり得ることが示唆された。
Local Immune Effector Cell-Associated Toxicity Syndrome(LICATS)の提唱(ポスター番号1537)
重症の全身性エリテマトーデス(SLE)、全身性強皮症(SSc)、特発性炎症性筋疾患(IIM)といった自己免疫疾患(AID)に対するCD19-CAR T細胞療法の進展に伴い、新たな毒性概念としてLICATS(Local Immune Effector Cell-Associated Toxicity Syndrome)が提唱された。本研究では、同療法を受けた39名のAID患者(SLE 20名、SSc 13名、IIM 6名)を対象に検討を行い、その77%にあたる30名において計54件のLICATSが報告された。
LICATSは、発熱や悪寒を伴う全身性のサイトカイン放出症候群(CRS)とは明確に区別され、過去に疾患の影響を受けた臓器において局所的に発生する、一過性の反応と定義される。発症時期の中央値は投与後10日(IQR 9-21日)、持続期間の中央値は11日であり、一貫してB細胞無形成(B-cell aplasia)のフェーズにおいてのみ発生した。主な罹患臓器は皮膚(35%)や腎臓(22%)、関節(19%)であり、その多くは軽症(Grade 1-2)であったが、6%にGrade 3(入院期間の延長)を認めた。
病態としては、罹患臓器からの免疫細胞の排除(cleansing)に伴う反応と考えられており、全例が低用量ステロイド等の使用により後遺症なく速やかに消失した。CAR T細胞療法を受けるAID患者の管理において、本病態を疾患の再燃と誤認せず、適切に記録・評価することが重要である。
食物繊維の摂取はメトトレキサートの治療効果を増すのか?(ポスターLB15)
関節リウマチ(RA)の病態には腸内細菌叢の乱れやTh17/Treg不均衡が関与し、メトトレキサート(MTX)の有効性も特定の腸内細菌や酪酸などの代謝産物に依存することが示唆されている。二重盲検RCT「Superfibre」では、安定したcsDMARDs継続下の活動性RA患者49名を対象に、イヌリン12g/日の30日間投与による効果を検証した。その結果、EULAR反応率は食物繊維群で53.85%、対照群で21.74%(p=0.040)であり、調整後の反応オッズ比は4.65(95% CI: 1.15-18.9、p=0.03)と有意な改善を認めた。特にMTX併用患者においてΔDAS28が-1.00(対照群は0.34)と顕著な改善を示し、治療効果とMTX使用の間に有意な交互作用(p=0.011)が確認された。免疫学的評価でも、食物繊維は血中Th17細胞数およびTh17/Treg比を有意に減少させており(p < 0.02)、腸管免疫軸を介した免疫バランスの回復が示された。本研究は、食物繊維がMTXの効果を増強する安価で安全な補助療法となる可能性を提示している。
以上限られたスペースの中での報告となったが、日々の臨床に役立つ情報が満載されていた会議であった。更なる情報は、web版で報告するので、ご興味のある方はご覧いただけると幸いである。
